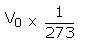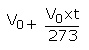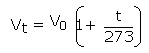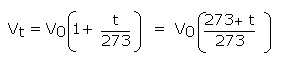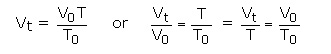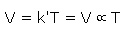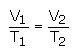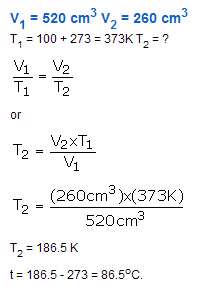|
اموزشی آخرین مطالب
آرشيو وبلاگ
شارل این قانون را درسال 1787 با دادن رابطه ای بین حجم و فشار یک گاز فرمول بندی کرد. این قانون بیان می کند که در فشار ثابت، حجم جرم معینی از گاز توسط 273/1 حجمش در دمای صفر درجه سانتی گراد برای هر یک درجه افت و خیز ، کاهش و یا افزایش می یابد. برای هر یک درجه افزایش در دما می باشد :
بنابراین، حجم کل در دمای t به صورت زیر در نظر گرفته می شود :
و یا به شکل ساده تر :
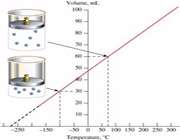
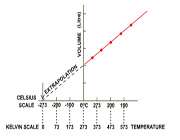
نموداری را می توان رسم کرد که در آن حجم در طول محور y و دما در طول محور x باشد و این نمودار، خطی راست را با عرض از مبدأ در نقطه ای روی محور y نشان می دهد:
زما نی که این خط را به سمت دماهای پایین تر برون یابی کنیم، این خط محور x را در جایی قطع خواهد کرد که به آن ، حجم در دمای صفر درجه سانتی گراد می گویند.
شکل 1- نمودار حجم در مقابل دما (تحت شرایط فشار ثابت)
دمایی که در آن حجم گاز صفر می شود دمای 273- درجه سانتی گراد است که مستقل از ماهیت و فشار گاز می باشد. پایین ترین دمایی که زیرآن حجمی وجود ندارد( منفی)، دمای صفر مطلق نامیده می شود و نیز اندازه گیری های دما بر اساس دمای صفر مطلق به عنوان مقیاس دمای مطلق یا مقیاس دمای کلوین شناخته می شود. در نتیجه قانون شارل را با توجه به مطالب مزبور می توان به شکل زیر فرموله کرد:
که در این جا 273+T = t نشان دهنده دما بر حسب کلوین و 273 = T0 می باشد.
بنابراین V / T ثابت می باشد. رابطه بالا ممکن است به شکل زیر نوشته شود:
در نتیجه حجم جرم معینی از گاز به طور مستقیم با دمای مطلق گاز در فشار ثابت متناسب است. اگر V1 حجم جرم مشخصی از گاز در دمای T1 و V2 حجم همان جرم از همان گاز در دمای T2 در فشار ثابت باشد، بنابراین می توان نوشت :
صحت قانون شارل را می توان با اندازه گیری حجم هایی از یک جرم معین ازگازی در دماهای مختلف در شرایط فشار ثابت تعیین کرد. در این بررسی ها در تمام مراحل مقدار V / T به صورت ثابت باقی می ماند. نمودار به دست آمده از نسبت حجم - دما در مقابل فشارهای مختلف، منحنی های هم فشار نامیده می شود. شارل همچنین ماهیت توسعه یافته ی گازهایی را با چگالی پایین توصیف کرد.
مسئله :یک نمونه از گاز هلیوم دارای حجم 520cm3 در دمای 100 درجه سانتی گراد می باشد. دمایی که در آن حجم گاز به 260cm3 می رسد را محاسبه کنید؟ فرض کنین که فشار ثابت است.
راه حل:
نظرات شما عزیزان: پيوندها
|
|||
|
|